Au cœur de la matière, deux types fondamentaux de transformations régissent son comportement : les transformations physiques et les transformations chimiques. Elles se distinguent par les modifications qu'elles infligent à la composition et à la structure des substances impliquées.
Une transformation physique altère l'état ou l'apparence d'une substance, mais sa composition chimique reste inchangée. La substance demeure fondamentalement la même, avant et après la transformation.
La fusion de la glace en eau liquide est un exemple paradigmatique. L'eau, sous forme solide ou liquide, reste constituée de molécules H₂O. Seul l'arrangement spatial de ces molécules diffère.
L'ébullition de l'eau est une autre illustration. L'eau liquide se transforme en vapeur d'eau, mais la formule chimique reste H₂O. La distance intermoléculaire augmente significativement.
La dissolution du sucre dans l'eau est également une transformation physique. Les molécules de sucre se dispersent dans l'eau, mais elles conservent leur structure moléculaire intacte. La solution reste une mixture de sucre et d'eau.
Le broyage d'un morceau de craie en poudre est une transformation physique. La composition chimique de la craie (carbonate de calcium) ne change pas. Seule la taille des particules est modifiée.
La magnétisation d'un morceau de fer est une transformation physique. L'alignement des domaines magnétiques à l'intérieur du fer est modifié, mais la composition chimique du fer (Fe) demeure constante.
Une transformation chimique, en revanche, implique la rupture et la formation de liaisons chimiques. De nouvelles substances, avec des propriétés différentes, sont produites. La composition chimique est fondamentalement modifiée.
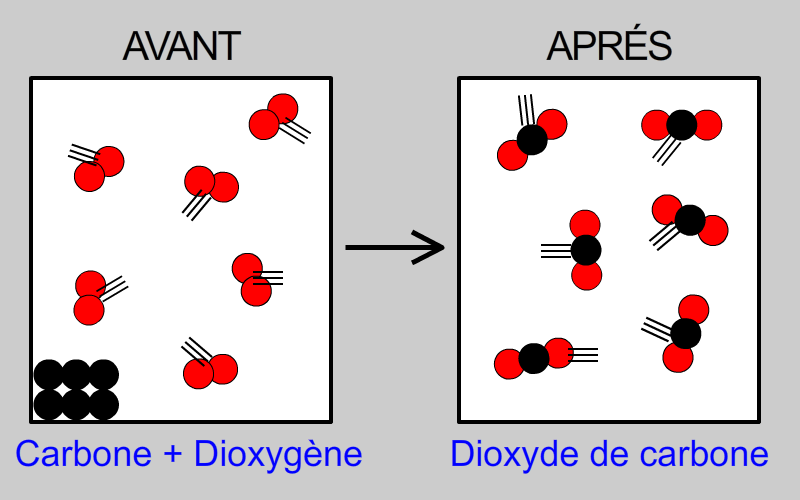
La combustion du bois est un exemple classique. Le bois réagit avec l'oxygène de l'air, produisant de la cendre, du dioxyde de carbone et de l'eau. Les liaisons chimiques présentes dans le bois sont brisées et de nouvelles liaisons sont formées.
La rouille du fer est une transformation chimique. Le fer réagit avec l'oxygène et l'eau de l'air, formant de l'oxyde de fer (rouille). La composition chimique du fer est modifiée, et une nouvelle substance est créée.
La cuisson d'un gâteau est une transformation chimique complexe. La chaleur provoque des réactions chimiques entre les ingrédients (farine, œufs, sucre), modifiant leur structure et leurs propriétés. Un nouveau produit, le gâteau, est formé.
La digestion des aliments est une série de transformations chimiques. Les enzymes catalysent la décomposition des molécules complexes (protéines, glucides, lipides) en molécules plus simples, absorbables par l'organisme.
La photosynthèse est une transformation chimique vitale. Les plantes utilisent l'énergie solaire pour convertir le dioxyde de carbone et l'eau en glucose et en oxygène. De nouvelles substances sont synthétisées.
Distinctions Clés
Les transformations physiques sont généralement réversibles. On peut reconvertir l'eau liquide en glace en abaissant la température. On peut évaporer l'eau et la recondenser.
Les transformations chimiques sont souvent irréversibles, ou nécessitent des conditions spécifiques pour être inversées. Il est difficile de reconvertir la cendre en bois. La rouille ne se transforme pas spontanément en fer.
Les transformations physiques impliquent des changements d'état ou de forme. Les transformations chimiques impliquent des changements de composition.
Les transformations physiques affectent les propriétés physiques, comme la densité, la viscosité, ou le point de fusion. Les transformations chimiques affectent les propriétés chimiques, comme la réactivité, l'acidité, ou le pouvoir oxydant.
L'énergie est souvent absorbée ou libérée lors des transformations chimiques. Ces transformations peuvent être exothermiques (libération de chaleur) ou endothermiques (absorption de chaleur). Les transformations physiques impliquent également des échanges d'énergie, mais généralement moins importants.
L'identification d'une transformation comme physique ou chimique repose sur l'analyse des substances impliquées avant et après la transformation. Si la composition chimique reste la même, il s'agit d'une transformation physique. Si la composition chimique est modifiée, il s'agit d'une transformation chimique.
La distinction entre ces deux types de transformations est cruciale pour comprendre le comportement de la matière et pour contrôler les processus chimiques et physiques dans de nombreuses applications scientifiques et industrielles. La chimie et la physique interagissent constamment pour décrire le monde qui nous entoure.
⌚🧪 Différence entre transformations physique et chimique ‖ Physique
-
difference transformation chimique et physique
-
difference transformation chimique et transformation nucleaire
-
difference transformation chimique et reaction chimique
-
différence transformation chimique et physique
-
différence réaction chimique et physique
-
difference entre transformation chimique et physique
-
difference entre reaction chimique et physique
-
difference entre une transformation chimique et physique
-
différence transformation chimique et réaction chimique
-
différence entre transformation chimique et réaction chimique