Bonjour à tous, passionnés de science ! Aujourd'hui, plongeons ensemble au cœur d'une réaction que l'on côtoie quotidiennement : la combustion du carbone. Vous vous êtes peut-être déjà demandé pourquoi on la qualifie de transformation chimique. Eh bien, préparez-vous, car on va explorer cela en détails !
Tout d'abord, il est crucial de comprendre ce qu'implique une transformation chimique. Il ne s'agit pas simplement d'un changement d'état physique, comme l'eau qui passe de l'état liquide à la glace. Non, une transformation chimique, c'est bien plus profond. Elle se caractérise par la formation de nouvelles substances. Ces nouvelles substances possèdent des propriétés radicalement différentes de celles des substances initiales. Des liaisons chimiques sont rompues et de nouvelles sont créées. C'est un véritable chamboulement au niveau moléculaire !
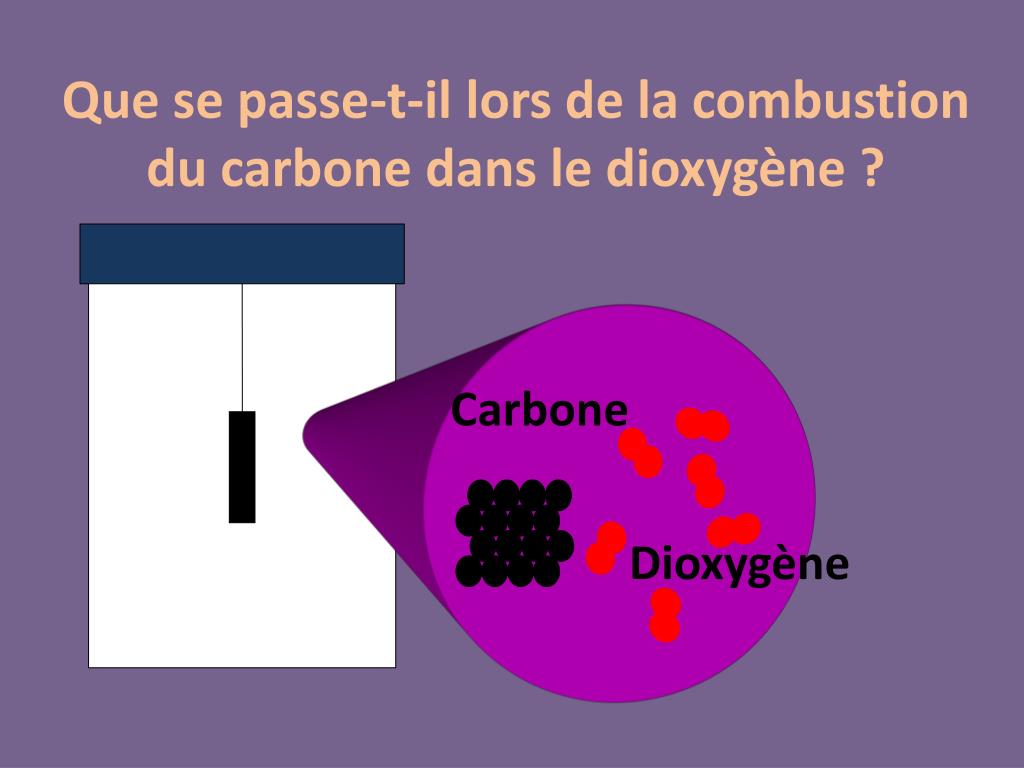
Dans le cas précis de la combustion du carbone, on part d'un élément simple : le carbone (C). On le trouve sous différentes formes, comme le charbon ou le graphite de nos crayons. Pour que la combustion ait lieu, il faut un autre acteur essentiel : le dioxygène (O2), présent dans l'air que nous respirons.
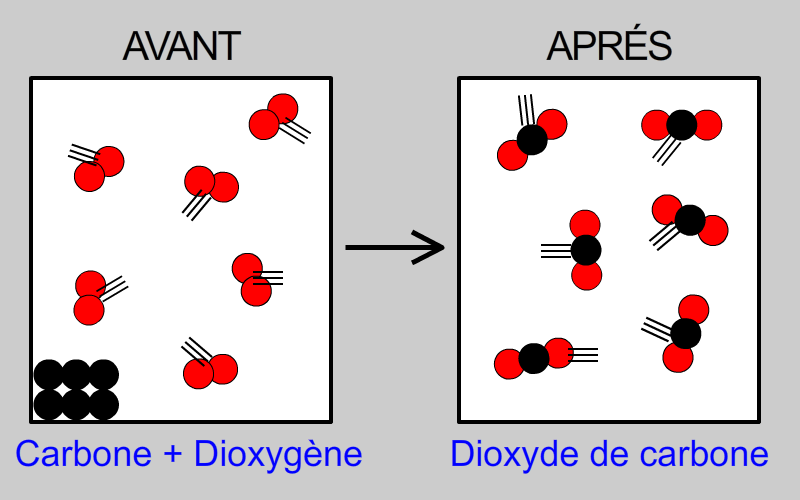
Lorsque le carbone et le dioxygène sont mis en présence à une température suffisamment élevée (c'est-à-dire quand on allume un feu !), une réaction spectaculaire se produit. Le carbone réagit avec le dioxygène. Cette réaction libère de l'énergie sous forme de chaleur et de lumière. C'est ce que l'on perçoit comme la flamme. Mais le plus important, c'est ce qui se passe au niveau des atomes.
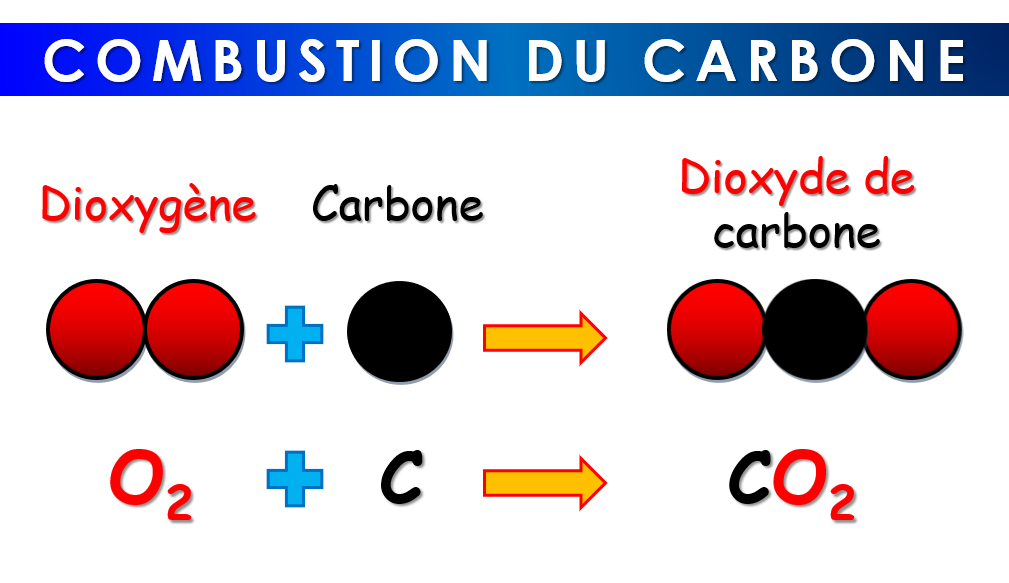
Le carbone et le dioxygène se combinent pour former une toute nouvelle molécule : le dioxyde de carbone (CO2). C'est un gaz incolore et inodore que nous expirons à chaque respiration. Le dioxyde de carbone n'a absolument rien à voir avec le carbone solide ou le dioxygène gazeux. C'est une entité moléculaire nouvelle avec des propriétés propres.
Zoom sur les liaisons chimiques
Pour bien comprendre, il faut imaginer les atomes comme des petites billes qui se tiennent par la main. Ces "mains", ce sont les liaisons chimiques. Dans le dioxygène, les atomes d'oxygène sont liés entre eux par une double liaison. Dans le carbone solide, les atomes de carbone sont liés entre eux d'une manière complexe, formant un réseau.
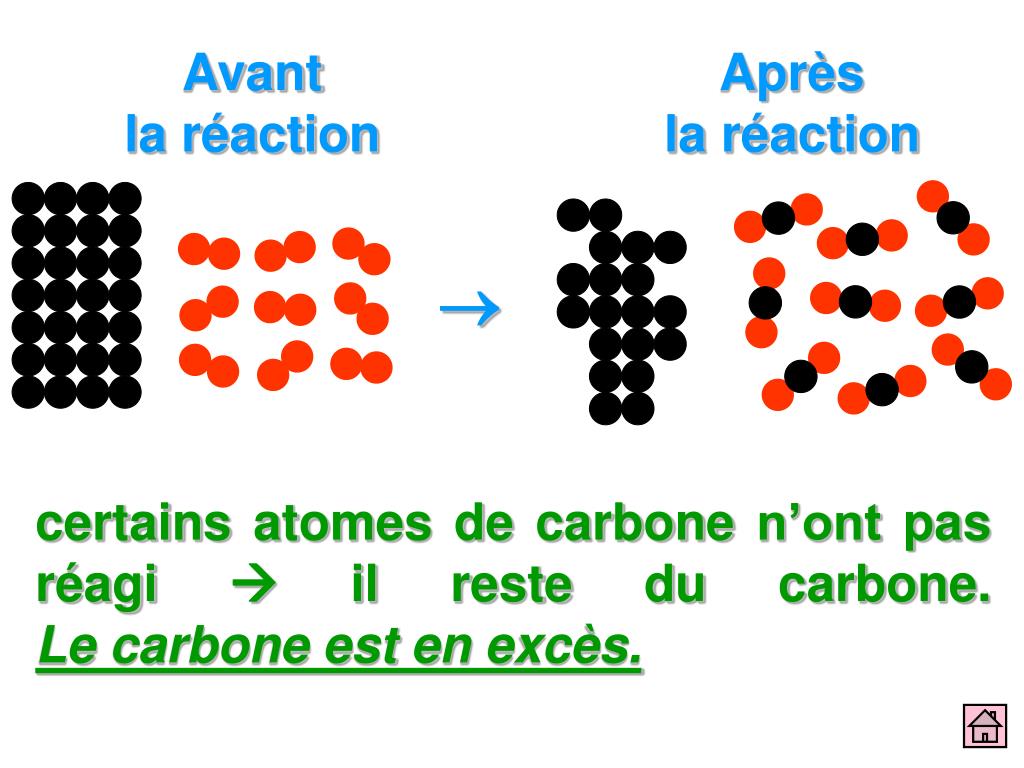
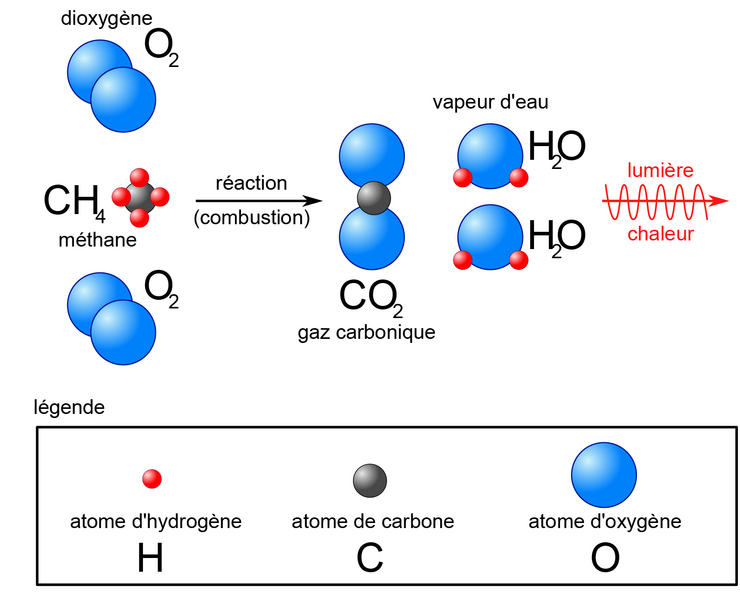
Lors de la combustion, les liaisons entre les atomes d'oxygène se brisent. Les liaisons entre les atomes de carbone se brisent aussi. Ensuite, de nouvelles liaisons se forment. Chaque atome de carbone s'associe à deux atomes d'oxygène pour former une molécule de dioxyde de carbone. C'est un remaniement complet de la structure moléculaire !
Les preuves irréfutables
Plusieurs observations confirment que la combustion du carbone est une transformation chimique.
- Apparition d'une nouvelle substance : On part de carbone solide et de dioxygène gazeux. On obtient du dioxyde de carbone gazeux. C'est clair, quelque chose de nouveau est apparu !
- Modification des propriétés : Le carbone est un solide, le dioxygène est un gaz qui permet la respiration. Le dioxyde de carbone est un gaz qui ne permet pas la respiration et qui contribue à l'effet de serre. Les propriétés ont changé radicalement.
- Libération d'énergie : La combustion dégage de la chaleur et de la lumière. C'est une indication que des liaisons chimiques se sont formées. La formation de liaisons chimiques libère de l'énergie.
- Réaction irréversible (dans des conditions normales) : Il est très difficile de transformer le dioxyde de carbone en carbone et en dioxygène spontanément. Cela nécessite des conditions très spécifiques et beaucoup d'énergie. Cela prouve que la réaction est allée dans un seul sens.
Alors, la prochaine fois que vous verrez une bûche se consumer dans la cheminée, pensez à cette transformation fascinante qui se déroule à l'échelle atomique. La combustion du carbone, bien plus qu'un simple feu, est une preuve éclatante de la puissance de la chimie !
En résumé, la combustion du carbone est bel et bien une transformation chimique car elle implique la formation d'une nouvelle substance (le dioxyde de carbone) avec des propriétés différentes de celles des réactifs (le carbone et le dioxygène), la rupture et la formation de nouvelles liaisons chimiques, et une libération d'énergie. J'espère que cette explication a éclairé votre lanterne ! À bientôt pour de nouvelles aventures scientifiques !
PPT - Combustion du carbone PowerPoint Presentation, free download - ID
-
pourquoi la combustion du carbone est-elle une transformation chimique
-
pourquoi la combustion du carbone est une transformation chimique
-
pourquoi la combustion du méthane est une transformation chimique
-
pourquoi la combustion du butane est une transformation chimique
-
pourquoi la combustion du carbone dans l air est elle lente
-
pourquoi la combustion du bois est une transformation chimique
-
pourquoi la combustion du charbon est une transformation chimique
-
pourquoi la combustion du butane est incomplète
-
pourquoi la combustion du butane est elle une transformation chimique
-
pourquoi la combustion de carbone est une transformation chimique