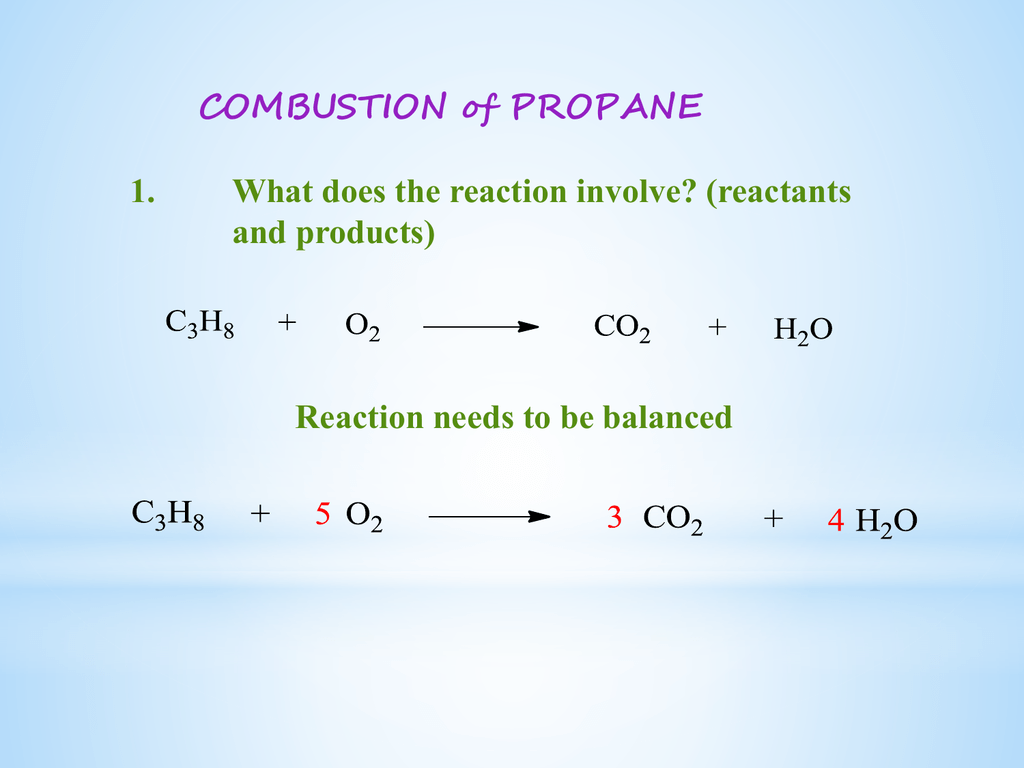
La combustion complète du propane (C3H8) est une réaction chimique exothermique. Elle produit du dioxyde de carbone (CO2) et de l'eau (H2O). L'équation chimique équilibrée est :
C3H8 + 5 O2 → 3 CO2 + 4 H2O
Chaque molécule de propane réagit avec cinq molécules de dioxygène. Cela produit trois molécules de dioxyde de carbone et quatre molécules d'eau.
Le propane est un alcane. Il est composé de trois atomes de carbone et huit atomes d'hydrogène. Sa combustion complète nécessite un apport suffisant de dioxygène.
L'équation ci-dessus est stœchiométrique. Elle indique les proportions exactes des réactifs et des produits. Elle est essentielle pour calculer les quantités impliquées.
Détails sur les réactifs
Le propane (C3H8) est un gaz incolore et inodore. Il est utilisé comme combustible. Sa densité est supérieure à celle de l'air.
Le dioxygène (O2) est un gaz essentiel à la vie. Il représente environ 21% de l'atmosphère terrestre. Il est indispensable pour la combustion.
Détails sur les produits
Le dioxyde de carbone (CO2) est un gaz incolore et inodore. Il est un produit de la respiration et de la combustion. Il contribue à l'effet de serre.
L'eau (H2O) est un liquide incolore et inodore. Elle est essentielle à la vie. Elle se forme sous forme de vapeur lors de la combustion.
Conditions de combustion
Une combustion complète nécessite un excès de dioxygène. Une combustion incomplète produit du monoxyde de carbone (CO) et de la suie (C). Le monoxyde de carbone est un gaz toxique.
La température d'inflammation du propane est d'environ 450°C. Un apport d'énergie est nécessaire pour initier la réaction.
La combustion complète libère une grande quantité de chaleur. Cette chaleur peut être utilisée pour chauffer ou produire de l'électricité.
Aspects thermodynamiques
La combustion du propane est une réaction exothermique. Elle libère de l'énergie sous forme de chaleur. L'enthalpie de réaction (ΔH) est négative.
La valeur de ΔH pour la combustion du propane est d'environ -2220 kJ/mol. Cela signifie que chaque mole de propane brûlée libère 2220 kilojoules de chaleur.
L'entropie du système augmente lors de la combustion. Le nombre de molécules de gaz augmente (6 molécules de réactifs deviennent 7 molécules de produits).
Implications pratiques
La combustion du propane est utilisée dans de nombreuses applications. Ces applications incluent le chauffage domestique, la cuisson, et la production d'électricité.
Les brûleurs à propane doivent être conçus pour assurer une combustion complète. Cela minimise la production de monoxyde de carbone.
La ventilation adéquate est cruciale. Elle permet d'évacuer les produits de combustion et d'assurer un apport suffisant d'oxygène.
Considérations environnementales
Le dioxyde de carbone est un gaz à effet de serre. Il contribue au réchauffement climatique. La combustion du propane contribue aux émissions de CO2.
Des technologies sont développées pour capturer et stocker le CO2. Ces technologies visent à réduire l'impact environnemental de la combustion.
L'utilisation de sources d'énergie renouvelables est une alternative à la combustion de combustibles fossiles.
Calculs stœchiométriques
Pour brûler 1 kg de propane, il faut environ 3,5 kg de dioxygène. Cela produit environ 3 kg de dioxyde de carbone et 1,6 kg d'eau.
Ces calculs sont basés sur les masses molaires des réactifs et des produits. Ils permettent de déterminer les quantités nécessaires et produites.
La connaissance de la stœchiométrie est essentielle pour optimiser les processus de combustion. Elle permet de minimiser les pertes et les émissions polluantes.
Sécurité
Le propane est un gaz inflammable. Il doit être manipulé avec précaution. Les fuites de propane peuvent provoquer des incendies ou des explosions.
Les détecteurs de propane sont recommandés dans les lieux où le propane est utilisé. Ils permettent de détecter les fuites et de prévenir les accidents.
Une formation adéquate est nécessaire pour manipuler le propane en toute sécurité. Il faut connaître les risques et les mesures de prévention.
En résumé, la combustion complète du propane est une réaction chimique bien définie. Elle produit du dioxyde de carbone et de l'eau. Elle libère une grande quantité de chaleur. Sa compréhension est essentielle pour de nombreuses applications et pour la sécurité. La stœchiométrie de la réaction est fondamentale. Les considérations environnementales sont importantes pour un avenir durable.
Les réactions de combustion - 1ère - Cours Physique-Chimie - Kartable
-
la réaction de combustion
-
réaction de combustion complète du propane c3h8
-
la réaction de combustion du propane
-
la reaction de combustion complete du propane c3h8
-
la réaction de combustion complète du propane
-
la réaction de combustion complète du propane c3h8
-
la réaction de combustion du méthane
-
definition de la reaction de combustion
-
la réaction chimique de la combustion